新光醫院腫瘤治療科 季懋欣醫師
癌症治療在近幾十年來有了長足的進步,但對於晚期癌症病人而言,仍然存在巨大挑戰。我最近在國際研討會的演講中,提到透過立體定位放射治療(SBRT) 與 樹突細胞(Dendritic Cell, DC)治療結合,想把法製造腫瘤「疫苗」,進而啟動全身性的抗癌。
DC是做什麼的呢?
DC就像免疫系統的「指揮官」,負責把蒐集到的抗原訊息告訴T細胞,讓T細胞去攻擊癌細胞。
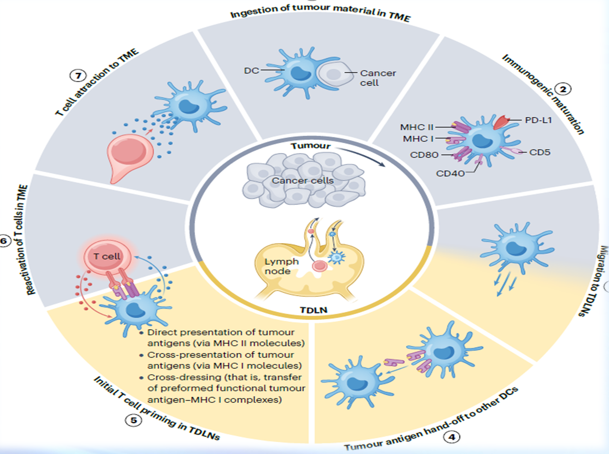
2. 強化: DC在抓到抗原後「成熟」。
3. 往淋巴結移動: 成熟的 DC 會移動到淋巴結。
4. 交棒給其他 DC: 在淋巴結裡, DC 會把腫瘤訊息再傳遞給「常駐的 DC」。
5. 訓練T 細胞: DC 把腫瘤抗原展示給 CD8⁺ T 細胞 和 CD4⁺ T 細胞,讓它們認識敵人並被激活。
6. 殺癌: 訓練好的 T 細胞,會循著 DC 釋放的化學訊號回到腫瘤,開始攻擊。
Nat Rev Clin Oncol. 2024 Apr; 21 (4): 257-277.
現在的DC療法碰到幾個困難:
- 做出來的細胞大多缺乏「cDC1」這個特別有效率的亞型,活化CD8⁺ T細胞的能力有限。
- 腫瘤周圍環境就是免疫抑制的,這也讓DC常常發揮不出功能。
cDC1:關鍵角色
在所有DC種類中,cDC1 特別重要。它們最擅長把腫瘤抗原呈現給 CD8⁺ T細胞,讓T細胞能殺死癌細胞。它們還能分泌 IL-12 和 CXCL9/10 這些訊號,維持免疫力的強度。未來若能直接製造或誘導更多cDC1,療效可能會更好。
放療怎麼幫忙?
除了殺死腫瘤,還能:
- 讓癌細胞死得「很吵」,釋放很多訊號,引起免疫注意。
- 把腫瘤抗原丟出來,幫助DC抓到目標。
- 吸引免疫細胞進到腫瘤裡,增加戰場兵力。
但壞消息是,放療同時也會讓癌細胞表現出更多 PD-L1(一種免疫煞車訊號),還會招來 Treg 和 MDSC 這些壞角色來壓制免疫反應。所以單靠放療還不夠,這時就需要DC來加強。
以前的臨床試驗:肝癌放療 + DC
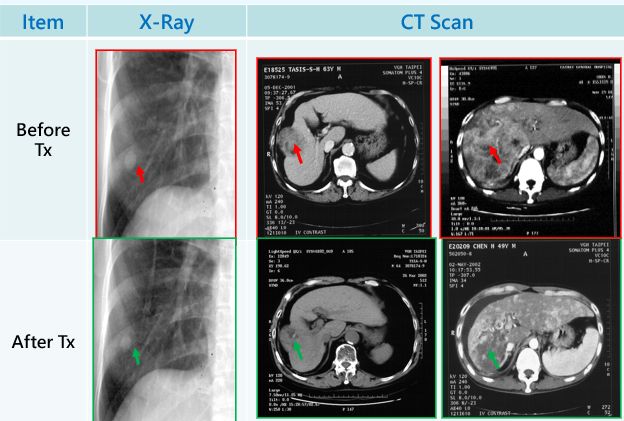
在我們進行的小型臨床試驗中,找了 14 位無法開刀或TACE的肝癌病人,進行腫瘤內的DC細胞注射。我們在注射的前2天進行兩次高劑量放療:
- 療效:6 位病人腫瘤達部分緩解,3 位AFP腫瘤指標下降超過一半。其中也有在轉移病人發現了遠端效應。
- 安全性:沒有嚴重副作用,僅有輕微發燒、倦怠或肌肉痠痛。
- 免疫反應:大多數病人都偵測到針對腫瘤抗原的免疫反應,還有部分病人NK細胞活性增加。
PSMA:一個很有潛力的靶點
PSMA 這個分子,不只在前列腺癌出現,也會出現在肝癌、膽管癌等腫瘤的新生血管上。研究發現:
- 放療可以讓PSMA表現更多、更一致。
- 如果能設計一種方法,把DC引導到PSMA表現的腫瘤血管,可能讓治療更精準、更有效。
這就像幫DC裝上導航系統,讓它們直達戰場的核心位置。我們實驗室目前也有研發出能夠綁定PSMA與cDC1的特定抗體,期望未來也能有所助益!
小結
愛因斯坦說的:「困難之中,必有機會。」「原位腫瘤疫苗」的概念,不是單純殺腫瘤,而是利用腫瘤本身去教免疫系統如何戰鬥。
很多臨床資料,SBRT + DC 是安全可行的,並且能啟動全身性的免疫反應。再加上 cDC1、PSMA標靶的發展並且合併免疫治療、其他局部治療方法,這條路可能會為晚期癌症病人帶來新的希望。
